君實生物特瑞普利單抗EXTENTORCH研究在國際權威期刊JAMA子刊發表
當地時間11月14日,由吉林省腫瘤醫院程穎教授牽頭開展的特瑞普利單抗聯合化療一線治療廣泛期小細胞肺癌 (ES-SCLC) 的III期EXTENTORCH研究結果發表在國際腫瘤學頂級期刊《美國醫學會雜誌·腫瘤學》 (JAMA Oncology,IF2023=22.5),為ES-SCLC一線免疫治療再添重磅循證醫學證據。程穎教授為本文的第一作者和通訊作者。
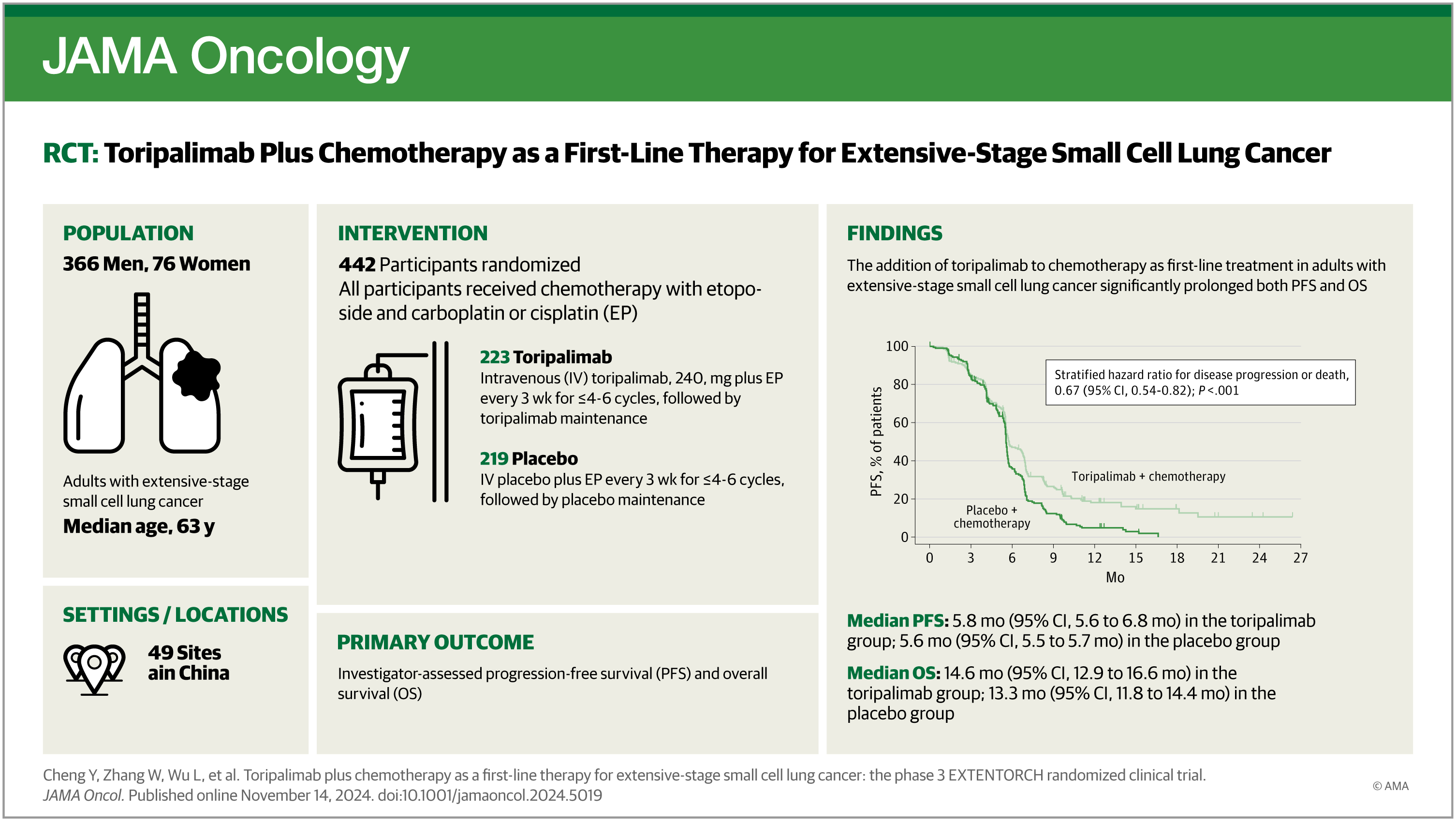
EXTENTORCH研究(NCT04012606)是一項多中心、隨機、雙盲、安慰劑對照的III期臨床研究,旨在比較特瑞普利單抗或安慰劑聯合依託泊苷及鉑類一線治療ES-SCLC的有效性和安全性。
EXTENTORCH研究主要研究者,吉林省腫瘤醫院程穎教授表示:“EXTENTORCH研究作為ES-SCLC領域全球首個成功達到預設雙主要研究終點陽性結果的抗PD-1單抗的Ⅲ期臨床研究,是ES-SCLC治療的又一次關鍵突破。 試驗組1年PFS率提升近4倍,所有亞組患者均有獲益,主要終點之一的OS取得陽性結果,成功通過了臨床“金標準”的考核,為患者帶來確切生存獲益。本次EXTENTORCH研究見刊不僅公佈了特瑞普利單抗聯合化療一線治療ES-SCLC的療效資料,更重要的是,這項研究進行了分子層面的探索,對篩選接受免疫治療的患者具有重要的指導意義。”
2023年5月,EXTENTORCH研究主要終點無進展生存期(PFS)和總生存期(OS)均達到方案預設的優效邊界,特瑞普利單抗由此成為全球首個在ES-SCLC一線治療III期研究中取得預設雙重主要終點陽性結果的PD-1抑制劑。
2024年6月,基於該研究的積極結果,特瑞普利單抗獲國家藥品監督管理局(NMPA)正式批准聯合依託泊苷和鉑類用於ES-SCLC一線治療,並獲中國臨床腫瘤學會(CSCO)兩大指南推薦為ES-SCLC一線治療優選方案,為中國ES-SCLC患者提供了治療新選擇。
此前,EXTENTORCH研究以口頭報告的形式在2023年ESMO大會上首次公佈了研究資料,此次全文發表於國際期刊,彰顯了國際學者對這項研究及特瑞普利單抗的肯定,結果顯示:
- 與單純化療相比,特瑞普利單抗聯合化療顯著改善患者PFS和OS,將疾病進展或死亡風險降低33%(HR=0.67;95% CI, 0.54-0.82),死亡風險降低了20%(HR=0.80;95% CI, 0.65-0.98)。亞組分析顯示,所有關鍵亞組均顯示出一致的PFS和OS獲益。
- 生物標誌物探索分析顯示,在特瑞普利單抗聯合化療組中,具有低腫瘤內異質性(ITH),HLA-A11+ HLA-B62–單倍型,KMT2D 和COL4A4野生型,或CTNNA2/SCN4A序列變異的患者的臨床獲益更明顯。
- 特瑞普利單抗聯合化療的安全性良好,未發現新的安全信號。兩組在治療期間出現的不良事件(TEAE,99.5%vs100%)和≥3級TEAE(89.6%vs89.4%)的發生率相似。
君實生物總經理兼首席執行官鄒建軍博士表示:“此次EXTENTORCH的重磅研究成果獲得《美國醫學會雜誌·腫瘤學》發表,體現了國際學術界對以特瑞普利單抗為代表的免疫治療在ES-SCLC患者一線治療中的價值認可。肺癌一直是公司重點關注的疾病領域,截至目前,特瑞普利單抗已成功獲批包括非小細胞肺癌(NSCLC)和小細胞肺癌(SCLC)在內的3項適應症,覆蓋了早中期(圍手術期)至晚期人群,管線內也還有其他產品正處於攻關階段,我們會積極推進相關工作,期待能為全球肺癌患者帶來更多更優的創新方案。”
1. 本材料旨在傳遞前沿資訊,無意向您做任何產品的推廣,不作為臨床用藥指導。
2. 若您想瞭解具體疾病診療資訊,請遵從醫療衛生專業人士的意見與指導。
關於EXTENTORCH研究
EXTENTORCH研究(NCT04012606)是一項多中心、隨機、雙盲、安慰劑對照的III期臨床研究,旨在比較特瑞普利單抗或安慰劑聯合依託泊苷及鉑類一線治療ES-SCLC的有效性和安全性。研究納入既往未接受系統治療的ES-SCLC患者,以1:1的比例隨機接受特瑞普利單抗(240mg, Q3W)或安慰劑聯合依託泊苷(100mg/m2, Q3W)和鉑類(順鉑 75 mg/m2或卡鉑 AUC 5 mg/mL/min, Q3W)治療4~6個週期,之後接受特瑞普利單抗或安慰劑維持治療,直至疾病進展、出現不可耐受的毒性或完成2年治療。研究分層因素包括性別和基線ECOG體能狀況評分。主要終點為研究者根據RECIST v1.1評估的PFS和OS。次要終點包括盲態獨立中心審查(BICR)評估的PFS、客觀緩解率(ORR)、疾病控制率(DCR)、疾病緩解率(DOR)和安全性等。探索性終點包括PD-L1的表達、腫瘤突變負荷(TMB)和其他基於測序的與臨床療效相關的生物標誌物。
自2019年9月至2021年5月,研究共納入442例ES-SCLC患者,隨機分配至特瑞普利單抗聯合化療組(n=223)或安慰劑聯合化療組(n=219)。該研究由程穎教授擔任主要研究者,在全國49家臨床中心聯合開展。
關於特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批准上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項專案支持,並榮膺國家專利領域最高獎項“中國專利金獎”。
特瑞普利單抗至今已在全球(包括中國、美國、東南亞及歐洲等地)開展了覆蓋超過15個適應症的40多項由公司發起的臨床研究。正在進行或已完成的關鍵註冊臨床研究在多個瘤種範圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批10項適應症:用於既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用於既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用於含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用於局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用於不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用於表皮生長因數受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用於可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用於中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依託泊苷和鉑類用於廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用於經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有6項獲批適應症納入《國家醫保目錄(2023年)》,是目錄中唯一用於治療黑色素瘤的抗PD-1單抗藥物。2024年10月,特瑞普利單抗用於復發/轉移性鼻咽癌治療的適應症在中國香港獲批。 在國際化佈局方面,特瑞普利單抗已作為首款鼻咽癌藥物在美國和印度獲批上市,其用於晚期鼻咽癌和食管鱗癌的一線治療獲得歐盟委員會批准上市。此外,英國藥品和保健品管理局(MHRA)受理了特瑞普利單抗聯合順鉑和吉西他濱用於局部復發或轉移性鼻咽癌患者的一線治療以及聯合紫杉醇和順鉑用於不可切除局部晚期/復發或轉移性食管鱗癌患者的一線治療的上市許可申請,澳大利亞藥品管理局(TGA)和新加坡衛生科學局(HSA)分別受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療後疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。
在國際化佈局方面,特瑞普利單抗已作為首款鼻咽癌藥物在美國和印度獲批上市,其用於晚期鼻咽癌和食管鱗癌的一線治療獲得歐盟委員會批准上市。此外,英國藥品和保健品管理局(MHRA)受理了特瑞普利單抗聯合順鉑和吉西他濱用於局部復發或轉移性鼻咽癌患者的一線治療以及聯合紫杉醇和順鉑用於不可切除局部晚期/復發或轉移性食管鱗癌患者的一線治療的上市許可申請,澳大利亞藥品管理局(TGA)和新加坡衛生科學局(HSA)分別受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療後疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。