君实生物特瑞普利单抗EXTENTORCH研究在国际权威期刊JAMA子刊发表
当地时间11月14日,由吉林省肿瘤医院程颖教授牵头开展的特瑞普利单抗联合化疗一线治疗广泛期小细胞肺癌 (ES-SCLC) 的III期EXTENTORCH研究结果发表在国际肿瘤学顶级期刊《美国医学会杂志·肿瘤学》 (JAMA Oncology,IF2023=22.5),为ES-SCLC一线免疫治疗再添重磅循证医学证据。程颖教授为本文的第一作者和通讯作者。
EXTENTORCH研究(NCT04012606)是一项多中心、随机、双盲、安慰剂对照的III期临床研究,旨在比较特瑞普利单抗或安慰剂联合依托泊苷及铂类一线治疗ES-SCLC的有效性和安全性。
EXTENTORCH研究主要研究者,吉林省肿瘤医院程颖教授表示:“EXTENTORCH研究作为ES-SCLC领域全球首个成功达到预设双主要研究终点阳性结果的抗PD-1单抗的Ⅲ期临床研究,是ES-SCLC治疗的又一次关键突破。 试验组1年PFS率提升近4倍,所有亚组患者均有获益,主要终点之一的OS取得阳性结果,成功通过了临床“金标准”的考核,为患者带来确切生存获益。本次EXTENTORCH研究见刊不仅公布了特瑞普利单抗联合化疗一线治疗ES-SCLC的疗效数据,更重要的是,这项研究进行了分子层面的探索,对筛选接受免疫治疗的患者具有重要的指导意义。”
2023年5月,EXTENTORCH研究主要终点无进展生存期(PFS)和总生存期(OS)均达到方案预设的优效边界,特瑞普利单抗由此成为全球首个在ES-SCLC一线治疗III期研究中取得预设双重主要终点阳性结果的PD-1抑制剂。
2024年6月,基于该研究的积极结果,特瑞普利单抗获国家药品监督管理局(NMPA)正式批准联合依托泊苷和铂类用于ES-SCLC一线治疗,并获中国临床肿瘤学会(CSCO)两大指南推荐为ES-SCLC一线治疗优选方案,为中国ES-SCLC患者提供了治疗新选择。
此前,EXTENTORCH研究以口头报告的形式在2023年ESMO大会上首次公布了研究数据,此次全文发表于国际期刊,彰显了国际学者对这项研究及特瑞普利单抗的肯定,结果显示:
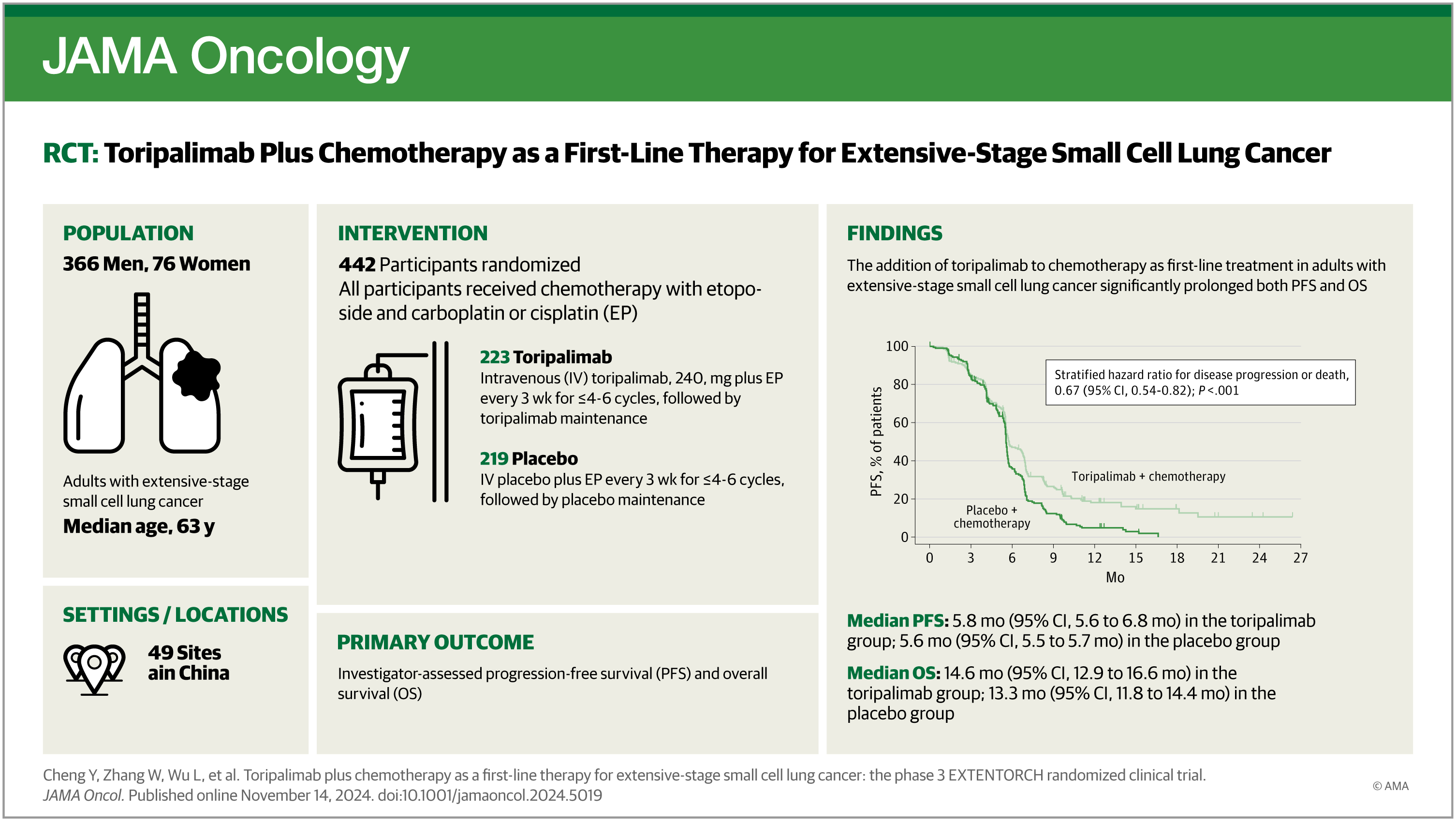
- 与单纯化疗相比,特瑞普利单抗联合化疗显著改善患者PFS和OS,将疾病进展或死亡风险降低33%(HR=0.67;95% CI, 0.54-0.82),死亡风险降低了20%(HR=0.80;95% CI, 0.65-0.98)。亚组分析显示,所有关键亚组均显示出一致的PFS和OS获益。
- 生物标志物探索分析显示,在特瑞普利单抗联合化疗组中,具有低肿瘤内异质性(ITH),HLA-A11+ HLA-B62–单倍型,KMT2D 和COL4A4野生型,或CTNNA2/SCN4A序列变异的患者的临床获益更明显。
- 特瑞普利单抗联合化疗的安全性良好,未发现新的安全信号。两组在治疗期间出现的不良事件(TEAE,99.5%vs100%)和≥3级TEAE(89.6%vs89.4%)的发生率相似。
君实生物总经理兼首席执行官邹建军博士表示:”此次EXTENTORCH的重磅研究成果获得《美国医学会杂志·肿瘤学》发表,体现了国际学术界对以特瑞普利单抗为代表的免疫治疗在ES-SCLC患者一线治疗中的价值认可。肺癌一直是公司重点关注的疾病领域,截至目前,特瑞普利单抗已成功获批包括非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC)在内的3项适应症,覆盖了早中期(围手术期)至晚期人群,管线内也还有其他产品正处于攻关阶段,我们会积极推进相关工作,期待能为全球肺癌患者带来更多更优的创新方案。”
1. 本材料旨在传递前沿信息,无意向您做任何产品的推广,不作为临床用药指导。
2. 若您想了解具体疾病诊疗信息,请遵从医疗卫生专业人士的意见与指导。
关于EXTENTORCH研究
EXTENTORCH研究(NCT04012606)是一项多中心、随机、双盲、安慰剂对照的III期临床研究,旨在比较特瑞普利单抗或安慰剂联合依托泊苷及铂类一线治疗ES-SCLC的有效性和安全性。研究纳入既往未接受系统治疗的ES-SCLC患者,以1:1的比例随机接受特瑞普利单抗(240mg, Q3W)或安慰剂联合依托泊苷(100mg/m2, Q3W)和铂类(顺铂 75 mg/m2或卡铂 AUC 5 mg/mL/min, Q3W)治疗4~6个周期,之后接受特瑞普利单抗或安慰剂维持治疗,直至疾病进展、出现不可耐受的毒性或完成2年治疗。研究分层因素包括性别和基线ECOG体能状况评分。主要终点为研究者根据RECIST v1.1评估的PFS和OS。次要终点包括盲态独立中心审查(BICR)评估的PFS、客观缓解率(ORR)、疾病控制率(DCR)、疾病缓解率(DOR)和安全性等。探索性终点包括PD-L1的表达、肿瘤突变负荷(TMB)和其他基于测序的与临床疗效相关的生物标志物。
自2019年9月至2021年5月,研究共纳入442例ES-SCLC患者,随机分配至特瑞普利单抗联合化疗组(n=223)或安慰剂联合化疗组(n=219)。该研究由程颖教授担任主要研究者,在全国49家临床中心联合开展。
关于特瑞普利单抗注射液(拓益®)
特瑞普利单抗注射液(拓益®)作为我国批准上市的首个国产以PD-1为靶点的单抗药物,获得国家科技重大专项项目支持,并荣膺国家专利领域最高奖项“中国专利金奖”。
特瑞普利单抗至今已在全球(包括中国、美国、东南亚及欧洲等地)开展了覆盖超过15个适应症的40多项由公司发起的临床研究。正在进行或已完成的关键注册临床研究在多个瘤种范围内评估特瑞普利单抗的安全性及疗效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、肾癌及皮肤癌等。
截至目前,特瑞普利单抗已在中国内地获批10项适应症:用于既往接受全身系统治疗失败的不可切除或转移性黑色素瘤的治疗(2018年12月);用于既往接受过二线及以上系统治疗失败的复发/转移性鼻咽癌患者的治疗(2021年2月);用于含铂化疗失败包括新辅助或辅助化疗12个月内进展的局部晚期或转移性尿路上皮癌的治疗(2021年4月);联合顺铂和吉西他滨用于局部复发或转移性鼻咽癌患者的一线治疗(2021年11月);联合紫杉醇和顺铂用于不可切除局部晚期/复发或远处转移性食管鳞癌患者的一线治疗(2022年5月);联合培美曲塞和铂类用于表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性、不可手术切除的局部晚期或转移性非鳞状非小细胞肺癌的一线治疗(2022年9月);联合化疗围手术期治疗,继之本品单药作为辅助治疗,用于可切除IIIA-IIIB期非小细胞肺癌的成人患者(2023年12月);联合阿昔替尼用于中高危的不可切除或转移性肾细胞癌患者的一线治疗(2024年4月);联合依托泊苷和铂类用于广泛期小细胞肺癌一线治疗(2024年6月);联合注射用紫杉醇(白蛋白结合型)用于经充分验证的检测评估PD-L1阳性(CPS≥1)的复发或转移性三阴性乳腺癌的一线治疗(2024年6月)。2020年12月,特瑞普利单抗首次通过国家医保谈判,目前已有6项获批适应症纳入《国家医保目录(2023年)》,是目录中唯一用于治疗黑色素瘤的抗PD-1单抗药物。2024年10月,特瑞普利单抗用于复发/转移性鼻咽癌治疗的适应症在中国香港获批。
在国际化布局方面,特瑞普利单抗已作为首款鼻咽癌药物在美国和印度获批上市,其用于晚期鼻咽癌和食管鳞癌的一线治疗获得欧盟委员会批准上市。此外,英国药品和保健品管理局(MHRA)受理了特瑞普利单抗联合顺铂和吉西他滨用于局部复发或转移性鼻咽癌患者的一线治疗以及联合紫杉醇和顺铂用于不可切除局部晚期/复发或转移性食管鳞癌患者的一线治疗的上市许可申请,澳大利亚药品管理局(TGA)和新加坡卫生科学局(HSA)分别受理了特瑞普利单抗联合顺铂/吉西他滨作为转移性或复发性局部晚期鼻咽癌成人患者的一线治疗,以及作为单药治疗既往含铂治疗过程中或治疗后疾病进展的复发性、不可切除或转移性鼻咽癌的成人患者的上市许可申请。